日前,真固生物关联公司及全球战略伙伴——Pillar Biosciences宣布,其oncoReveal™ Dx肺癌结直肠癌基因检测试剂盒获得美国食品药品监督管理局 (FDA)上市批准。该产品是一种基于组织的 NGS 伴随诊断检测试剂盒,用于检测非小细胞肺癌 (NSCLC) 和结肠直肠癌 (CRC) 肿瘤DNA中的体细胞突变。在此之前,该试剂盒已经获得了CE认证。
“上海真固生物有限公司作为Pillar Biosciences唯一的全球战略合作伙伴和国内唯一的全部技术和全系列产品授权转化及代理服务商,已经将其SLIMamp扩增子建库技术和PiVAT生信分析系统完整转化到国内应用市场上,造福更多中国肿瘤患者。在此基础上,真固生物也将立即启动oncoReveal™ Dx产品的进口注册工作。”
“真固生物本身也拥有即将于年底获证的国内注册NGS产品(进展见文末),相信在不久的将来,真固生物将成为国内唯一拥有国产及进口注册双证NGS肿瘤伴随诊断试剂盒的精准诊断企业!”
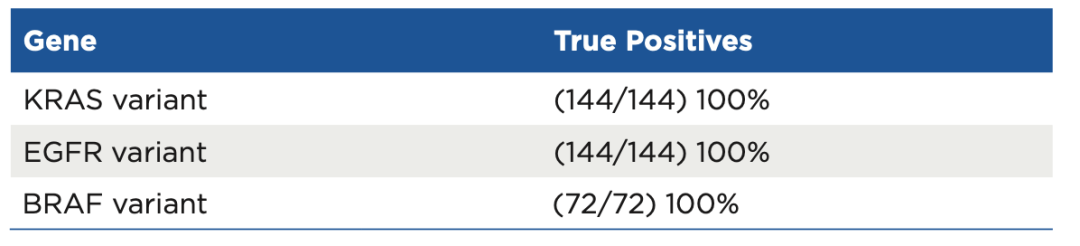
测试样本来自于NSCLC 和 CRC 患者的FFPE 样本,并使用 oncoReveal™ Dx 肺癌和结肠癌检测进行了临床验证和验证研究。该测定证明与 FDA 批准的 cobas®EGFR 突变测试和 FDA 批准的 therascreen®KRAS 测试结果一致。
研究团队在3个临床试验基地进行了oncoReveal™ Dx 肺癌和结肠癌检测的重现性评估,每个地点的 2 名操作员在非连续的日子里操作 3 次试验,每个站点使用一台测序仪和两批试剂,每个小组成员在每次运行中以 4 次重复进行测试,总共有 360 个可能的结果,且所有结果呈现出100%的重现性。

测序平台
oncoReveal™ Dx肺癌结直肠癌试剂盒采用同样经FDA批准、适用于IVD的Illumina MiSeq™ Dx平台进行NGS检测,为临床医生和临床实验室提供全面可靠的DNA测序结果。
☑ 一步检测,辅助多种靶药治疗方案
- 指导非小细胞肺癌(NSCLC)患者EGFR TKI疗法
- 指导转移性结直肠癌(mCRC)患者Erbitux®(西妥昔单抗)或Vectibix®(帕尼妥单抗)靶向治疗
☑ 极速检测流程
- 单管建库+两步扩增
- 从提取到测序不到8小时
- 从提取到报告生成仅需4个自然日
☑ 极其灵敏和稳定的反应体系
- 仅需要 30 ng DNA 建库
- 仅 30% 的肿瘤细胞占比即可准确检出
- 高达 50% 的污染坏死组织也可精准检出
☑ 强大的生物信息学分析系统
- 检测低至 3.0% VAF 的临床相关变异
- 运行时间 <8 小时
上海真固生物科技有限公司由位于上海和波士顿的创始人共同创立,是一家兼具中国文化基因和国际科技背景的精准医疗技术公司,公司致力于以高通量测序文库制备技术及配套的数据分析与解读系统为核心的临床级精准诊断整体解决方案的研发与应用。公司拥有成熟的针对gDNA、FFPE DNA、 cfDNA等的高通量测序“一管”文库制备技术和基于RNA的融合基因检测技术,大幅降低了检测试剂盒的成本。与试剂配套的易学易用的生物信息学分析软件,可以“一键”完成从原始数据到突变列表注释的全部数据分析流程。同时提供从样本提取到自动化报告的全流程自动化、“一体化”院内LDT/IVD整体解决方案。综合技术优势和成本优势的叠加,有效解决了当前高通量基因测序技术在应用推广过程中存在的效率低、准确率低、流程复杂、成本高等障碍,使高通量测序可以在院内实现“一天”级实验流和两天级工作流。有效推动了基因检测在肿瘤、遗传病等领域的普及应用与发展。从而实现精准医疗大众化,惠及国人健康。
电话|021-6089 0178
本文由 SEQ.CN 作者:白云 发表,转载请注明来源!








